CRISPR Gen Düzenleme Yöntemi Nedir? CRISPR-Cas9 Sistemini Kullanarak Genleri Nasıl Düzenleriz?
Prokaryotlarda Hücre Savunması ve Evriminden, Ismarlama Bebeklere...

- İndir
- Dış Sitelerde Paylaş







“Doğa bir savaş alanıdır.” sözünü, çayırlarda koşturan aslan ve geyiklerden çok, bağışıklık sisteminde yaşananlar olarak anlamak mümkündür. Moleküler düzeydeki evrimsel savaşın en serti patojenler (yani hastalık yapan organizmalar) ile konak canlıların bağışıklık sistemi arasında gerçekleşmektedir desek abartmış olmayız. Birlikte evrimin en güzel örneklerini görebileceğimiz bu çekişme, aslında temel olarak bir organizmanın “ben ve diğerleri” ayrımını yapabilmesine dayanmaktadır. Patojenler için evrimsel başarı ise bu ayrımdan kaçabilmelerine bağlıdır.
Modern tıbbın önlenebilir hastalıklara karşı bağışıklık sistemimiz kadar iyi bir iş çıkardığını reddedemeyiz. Tedavi ve aşı yöntemleri sayesinde (ve tabi ki gıda, temizlik gibi birçok faktörün de birleşimi ile) insan ömrü 1900’lerin başından bu yana iki katına çıkmıştır. Fakat elbette bu bağışıklık sistemlerini araştırmayı bir kenara bırakacağımız anlamına gelmiyor. Henüz çare bekleyen birçok hastalığın yanında aslında bu sistemler birazdan da anlatmaya çalışacağımız gibi hiç tahmin edemeyeceğimiz teknolojik yeniliklere yol açabilir ki zaten temel bilim çalışmalarının tamamı böyle değil midir?
1950’lerin başında Rosalind Franklin, Francis Crick ve James Watson DNA’nın kimyasal yapısını keşfettiler. Bu insan genlerinin kimyasal modifikasyonu yoluyla iyileştirilebilmesinin bir başlangıcıydı. Bu keşif, genetik biliminin en büyük sıçramalarından biriydi. Franklin, Watson ve Crick genetik kökenli hastalıkların tedavisi için bilim insanlarının önünü açarak tıp dünyasında yeni bir kapı aralanmasına yardım etti. Bu, aynı zamanda güne yeni umutlarla açılan gözler için de kalıtsal hastalıkların tedavisinin bulunması demekti.
Her gün bulunan yeni bilgiler, bilim insanlarını şaşkınlıkla birlikte daha fazla meraka ve araştırmaya sürüklüyor. Bilim insanları araştırmaya devam ettikçe bilim öyle bir noktaya geldi ki, bir yerde insanların gözünde umut oluyorken bir yerde silah, savaş ve gözyaşı oluyor. Bilim işte bu. Bazen belli belirsiz bazen sert ve düzgün çizilmiş bir garip çizgi…
Bağışıklık Sistemini Tanıyalım
Öncelikle kısaca bağışıklık sistemini tanıtmak faydalı olur. Bahsettiğimiz gibi bağışıklık sistemi bir organizmanın kendi hücrelerini yabancı hücreler ve maddelerden ayırabilmesi ve bunları etkisiz hale getirebilmesi adına özelleşmiş hücre, protein ve etki mekanizmalarının tümüne verilen addır. Bu sistemi temel olarak ikiye ayırabiliriz; doğuştan gelen bağışıklık ve edinilmiş bağışıklık. Doğuştan gelen bağışıklık evrimsel olarak daha eskidir ve tüm canlılarda bulunur. Bu sistemin elemanları, bakterilerde işgalci virüs DNA’larını kesen nükleaz enzimleri olabildiği gibi bizlerde vücuda giren yabancı maddeye ilk tepkiyi veren fagositler, mast hücreleri gibi hücreler de olabilir. Bu yazının esas konusu ve üzerinde daha detaylı duracağımız sistem ise edinilmiş bağışıklık sistemidir.
Edinilmiş bağışıklık sistemi üzerine küçük bir araştırma yapmak bile insanı heyecanlandırmaya yeter aslında. Bu sistemin özelliği ileri düzeyde özelleşmiş, neredeyse her patojeni tanıyabilecek potansiyele sahip hücrelerden ve bir sefer tanıdığı patojeni uzun zaman hafızasında tutabilecek (mekanik bir hafızadan bahsediyoruz) etki sistemlerinden oluşmasıdır. Bazı aşıların insan ömrü boyunca tek bir sefer yapılmasının yeterli olmasının sebebi de bu hafızadır. Edinilmiş bağışıklığın omurgalılara has bir sistem olduğu söylese de diğer canlılarda da bu tür benzer sistemlerin ipuçlarını görebiliyoruz, özellikle birazdan bahsedeceğimiz gibi.
İnsandaki ve daha genel anlamda omurgalılardaki edinilmiş bağışıklık sistemini biraz detaylandıracak olursak T ve B hücrelerinden bahsetmemiz gerekli. Bu hücreler birbirlerine oldukça benzeseler de bir enfeksiyon durumunda aktif hale geçmelerinin ardından önemli farklılıklar göstermeye başlarlar. T hücreleri patojen ile girdikleri doğrudan hücre etkileşimi ile savunmada görev alırlar. Kimi T hücreleri yardımcı olarak adlandırılır ve diğer savunma hücrelerinin enfekte olmuş bölgeye çağırılmasında görev alır, kimileri ise katil olarak adlandırılır ve bakterilerin veya enfekte olmuş insan hücrelerinin yok edilmesini sağlar. B hücreleri ise mutlaka bir şekilde duymuş olduğunuz antikor denilen maddelerin üretiminde temel görevi üstlenen hücrelerdir. Antikorlar, Y şeklindeki proteinlerdir ve en önemli özelliği patojenlerin tanınmasına olanak sağlaması ve hatta bazı durumlarda bu patojenleri öldürebilmesidir.
Bu noktada biraz teknik ayrıntıya girmek, sistemin heyecan verici yanını anlamamıza yardım edecek. Antikorlar, antijen denilen ve bakteri ve virüslerin yüzeyinde bulunan maddelere bağlanarak işaretleme yaparlar. Antijenler özel maddeler olmak zorunda değildir, yani eğer bir antikor bakterinin yüzeyinde, bakteriye özgü herhangi bir proteine bağlanıyorsa artık o protein antijen olarak adlandırılır. Burada “herhangi” kelimesi önemlidir çünkü antikorların “herhangi” bir yabancı proteini tanıyabilecek çeşitlilikte olması gerekir. Bu çeşitliliğin kaynağı ise –evet, doğru tahmin ettiniz– mutasyonlardır.
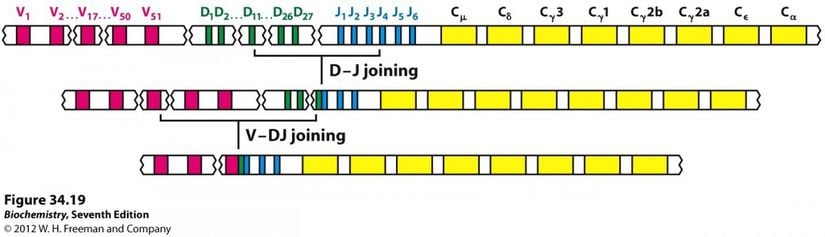
Bir B hücresinin olgunlaşması aslında bize evrim sürecinin minik bir sunumunu verir diyebiliriz. Olgunlaşmamış B hücrelerinin tamamı, diğer vücut hücrelerimizle birlikte aynı genetik yapıya sahiptir. Fakat olgunlaşma sürecinde özellikle antikorların antijen ile etkileşen kısımlarının üretiminden sorumlu gen bölgeleri yani VDJ genleri önemli değişiklikler yaşar. Bu değişimlerden biri somatik hipermutasyon dediğimiz süreçtir. Antikorların antijen ile bağ kurabilmesinin temeli, 3 boyutlu şekillerinin birbirlerine olan uyumudur, bunu bir anahtar-kilit analojisi ile anlamaya çalışmak en kolayıdır. İşte somatik hipermutasyon da bir antikorun antijen ile bağ kuran aktif bölgesini (yani bizim anahtarımızın tırtıklı yüzeyini) rastgele bir şekilde değiştirmeye yarar. İstatistiksel olarak somatik hipermutasyona maruz kalan bölgelerdeki mutasyon oranı, vücudumuzun diğer bölgelerine oranla 1.000.000 kat daha fazladır - ki bu da her yeni B hücresinin birkaç adet mutasyon taşıdığı anlamına gelir.
Bir diğer değişim ise VDJ rekombinasyonları veya somatik rekombinasyon denilen süreçtir. VDJ genleri olgunlaşmamış bir B hücresinde çok çeşitli sayıda bulunurken (VVVVV DDDD JJJJJJ gibi) hücrenin olgunlaşması sırasında rastgele bir şekilde seçilerek sayıları tek bir antikor üretebilecek kadar azaltılır (VVDJ).
Bu iki süreç sonunda ise her bir olgunlaşmış B hücresinin farklı bir antikor üretebildiği bir hücre havuzu elde etmiş oluruz. Elimizdeki bu çeşitliliğin üzerindeki seçilim baskısı ise antijenler tarafından oluşturulur. Ürettiği antikor, bir antijene bağlanabilen B hücreleri seçilir ve bağışıklık hafızası dediğimiz mekanizma ile korunurlar. Aynı patojen ile tekrar enfeksiyon durumunda hızlı bir şekilde çoğaltılarak çok daha çabuk ve etkili tepki verilmesini sağlarlar. Diğer B hücreleri ise ömürlerini tamamlayana kadar vücutta dolaştıktan sonra yok edilirler.
İşte size ekolojik anlamda kullandığımızın aynısı olmasa da sadece en uyumluların hayatta kaldığı bir evrimsel süreç örneği! Tabii burada bu süreçlerin somatik olduğunu yani vücut hücrelerinde gerçekleştiğini ve yavrulara aktarılmadığını belirtmek gerekir. Zaten bu sebeple edinilmiş bağışıklık sistemi, canlının ömrü boyunca karşılaştığı patojenlere karşı direnç sağlar.
Prokaryotların Dünyasına Yolculuk
Şimdi gelin üzerinde konuştuğumuz boyutu değiştirelim ve prokaryotların yani zarlı organel bulundurmayan tek hücreli canlıların dünyasına girelim.
Evrimsel olarak canlılığı en temel düzeyde 3 gruba ayırırız. Bunlardan biri ökaryotlardır ki çevrenizde görebildiğiniz canlıların tamamı bu gruba dâhildir. Bir diğeri bakterilerdir, birçoğumuz bakterilere de aşinayız. Fakat 3. grup olan arkeleri çok tanıdığımız söylenemez. Bu aslında doğal çünkü uzun bir süre boyunca arkeler bakteriler grubuna dâhil edilmişti. Ta ki 1977 yılında, ünlü mikrobiyolog Carl Woose 16S ribozomal RNA benzerliklerini incelemesinin ardından onları ayrı bir grup olarak tanımlayana kadar...
Geçen 35 yıl boyunca arkeler üzerinde birçok çalışma yapıldı ve bugün Carl Woose’un önerdiği 3 gruplu sınıflandırma sisteminin oldukça tutarlı olduğunu biliyoruz. Daha da önemlisi evrimsel açıdan arkeler ve ökaryotların birbirlerine bakterilerden daha yakın olduğunu da biliyoruz. Şöyle ki her ne kadar arkeler, prokaryot canlılar olsa da DNA eşleme, protein sentezi gibi işlevleri gerçekleştirirken kullandıkları proteinler bakterilerden çok ökaryotların proteinlerine benzemekte. Hatta bu benzerlik ve arkelerin etkili DNA tamir sistemlerinden faydalanarak bu canlıların kanser araştırmalarında kullanılması ile ilgili çalışmalar yürütülmekte.
Prokaryotlarda Hücre Savunması
Bu ön bilgiler eşliğinde, daha fazla dağılmadan konumuza dönelim. Patojenlerin oluşturduğu sıkıntılar maalesef tek hücrelilerin dünyasını da sarmış durumda. İster insan bağırsağında yaşayan bir bakteri olun ister 75 derecede aşırı asidik ortamda yaşayan bir arke, başınız asla virüslerden kurtulmaz. Bu da doğal olarak tek hücreli canlıların da virüslere karşı bir savunma mekanizmasına sahip olmasını zorunlu kılar.
Virüslerin etki mekanizmasını kısaca şöyle özetleyebiliriz: Virüslerin yüzey proteinlerini kullanarak hücreye tutunması, kendi genetik materyalini konak hücrenin içine aktarması, bu genetik materyalin, hücrenin protein sistemini kullanarak kendini eşlemesi ve sonunda oluşan çok sayıda yeni virüs sebebi ile konak hücrenin patlaması ve virüslerin yeni konaklar bulmak üzere dağılması. Bakteri ve arkelerin doğuştan gelen bağışıklık sistemi genellikle virüslerin tutunduğu reseptörlerin yapısını değiştirmek ve restriksiyon – modifikasyon enzimleri yardımı ile hücrenin DNA’sına girmiş virüs DNA’sını kesmek şeklinde işliyor. Ancak son zamanlarda yapılan çalışmalar ile bu canlıların bir de edinilmiş bağışıklık mekanizmasına sahip olduğu ortaya çıktı. Evet, yanlış duymadınız. Sadece omurgalılara özgü olduğunu düşündüğümüz edinilmiş bağışıklık sistemi, talihsiz bir şekilde “ilkel” olarak nitelendirdiğimiz prokaryotlarda da bulundu.
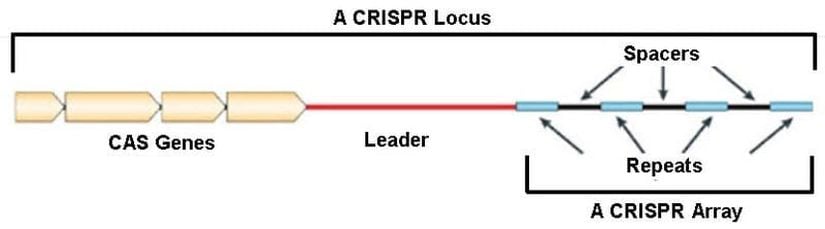
Bilinen arkelerin tamamına yakınında ve bakterilerin de yarısında bulunan bu sistem CRISPR-Cas sistemi olarak adlandırılıyor. CRISPR’ın açılımı “clustered regularly interspaced palindromic repeats”. Henüz bir Türkçe karşılığına denk gelmedim, o sebeple ilk çeviri önerisini burada sunup “Düzenli Aralıklarla Bölünmüş Palindromik Tekrar Kümeleri” diyebilirim. CRISPR denildiğinde kastedilen teknik anlamda canlının DNA dizisi üzerinde, CRISPR lokusunu tanımlayan gen dizileridir. Bunlar cas genleri, onu takip eden lider dizi ve sonrasında gelen tekrar (repeat) ve aralık (spacer) dizileridir. Tekrar dizileri bir canlı için tamamen aynı olmakla birlikte bu tekrarların arasındaki aralık dizileri birbirinden farklılık göstermektedir. Cas ise bu bağışıklık sisteminde görev alan proteinlerin genel adıdır.
 ASM Blog
ASM BlogCRISPR kümelerinin varlığı 1980’lerden beri bilinse de canlının savunma mekanizmasındaki rolü görece yeni kanıtlanmış durumda. Bu çıkarıma giden araştırmalar ise 2005 yılında CRISPR genleri üzerine çalışan 3 farklı grubun keşfi ile başladı. Bu grupların keşfettiği şey, CRISPR kümelerinde bulunan aralık genlerinin, o canlıyı enfekte eden bazı virüsler ile aynı diziye sahip olmasıydı. Ayrıca bir virüs DNA’sı ile aynı diziye sahip aralık genine sahip olmak o virüse karşı bir direnç veriyordu. Elbette buradan CRISPR sisteminin nükleik asit temelli bir bağışıklık mekanizması olabileceği hipotezi ortaya çıktı ve yapılan araştırmalar sonucunda bugün bu hipotezin büyük oranda doğrulanmış olduğunu söyleyebiliriz.
Emmanuelle Charpentier, George Church ve Jennifer Doudna, CRISPR üzerine çalışan ve bilime önemli katkılar sağlayan bilim insanlarıdır. 2012 yılına gelindiğinde Jennifer Doudna öncülüğündeki ekip bir canlının DNA'sını kesebilecek, izole edebilecek ve düzenleyebilecek bir sistem geliştirdi. Yani aktif bir Cas9 proteini, DNA’yı yüksek hassaslıkta ve doğrulukta kesebilmeleri için gereken tek şey o DNA’nın dizisini kesebilecek bir makastı. Bundan hareketle DNA’nın bu baz dizisine denk gelen RNA molekülü oluşturuldu ve bu RNA molekülü Cas9 proteini ile birleştirilerek bir kompleks meydana getirildi.
CRISPR-Cas9 teknolojisi istenilen DNA bölgesinden kesim yapabilmeyi sağlıyor. Bakterilerin bazılarının bünyelerinde CRISPR-Cas9 sistemine benzer bir gen düzenleme sistemi doğal olarak bulunur. Bakteriler bu sistemi işgalci patojenlere, örneğin virüslere karşı yanıt olarak kullanır; bir bağışıklık sistemi gibi... CRISPR kullanarak bakteriler virüs DNA’sından parçalar çıkarır ve bir daha saldıracak olursa virüsü tanımalarına ve savunmaya geçmelerine yardımcı olması için birazını saklarlar.
Bugün, bu moleküler makineyi tamamen farklı bir amaç için uyarladık: Bir organizmanın DNA kodunda seçilen harfleri değiştirmek için...
CRISPR Nasıl Çalışır?
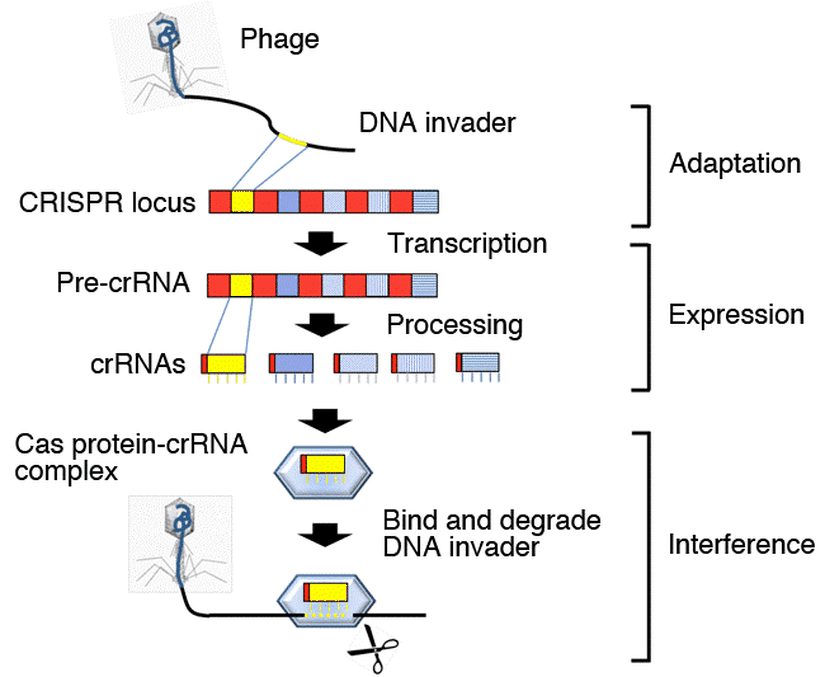
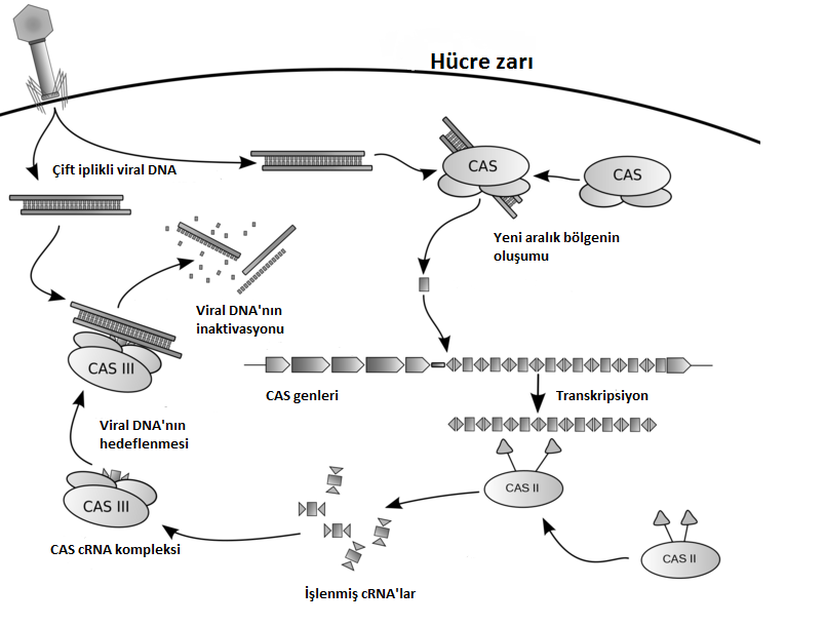
Genel hatları ile sistemi şu şekilde özetleyebiliriz: Öncelikle organizma bir virüs tarafından enfekte edilir. Ardından bu virüsün DNA’sı hücre tarafından parçalanır ve bu parçalar arasından bir ön-aralık (protospacer) geni seçilir. Seçilen bu gen çeşitli proteinler tarafından işlendikten sonra CRISPR lokusunda lider genin hemen sonrasına, yeni bir tekrar geni ile birlikte eklenir ve aralık geni adını alır. Bu da bize neden aralık genlerinin birbirinden farklı olduğunu anlatıyor; çünkü her biri farklı bir virüsten alınmış. Daha sonra bu tekrar ve aralık bölgelerinden sentezlenen CRISPR RNA’lar (crRNA) belirli Cas proteinlerinin de yardımı ile kesilir ve işlenir. İşlenmiş crRNA’lar başka Cas proteinleri ile birleşerek CRISPR ribonükleoprotein komplekslerini (crRNP) oluşturur. Hücrenin aynı virüs ile tekrar enfekte edilmesi durumunda ise virüsün DNA’sına karşılık gelen aralık dizisini taşıyan crRNP’ler virüs DNA’sını tanır ve Cas proteinlerinin nükleaz aktivitesi ile yabancı DNA parçalanır.
 Spring8
Spring8Cas proteinlerini de bu sisteme uygun olarak 4 gruba ayırabiliriz. İlki yeni karşılaşılan virüslerden aralık genlerinin elde edilmesini sağlayan nükleaz ve rekombinaz proteinleri. İkincisi crRNA işlenmesinde görev alan ribonükleaz enzimleri. Üçüncüsü olgun crRNA’lar ile bağ kurup crRNP oluşturulmasını sağlayan ve yabancı DNA’nın tanınmasında rol alan proteinler. Dördüncüsü de yabancı DNA’ların parçalanmasını sağlayan nükleazlar.
Araştırmalar bize CRISPR-Cas sistemlerinin temel olarak 3 gruba ayrılabileceğini gösteriyor. Tip 1, 2 ve 3 olarak adlandırılan bu sistemlerden Tip 1 ve 3 birbirlerinden filogenetik olarak oldukça uzak birçok bakteri ve arkede bulunmakla birlikte tip 2 sistemlere sadece bakterilerde rastlanmış. Ayrıca bazı plazmidlerde de CRISPR-Cas sistemlerini bulmak bize bu sistemlerin sıklıkla yatay gen transferi aracılığı ile paylaşıldığını gösteriyor. Tabi ki bu da sistemin kökenine ilişkin evrimsel çalışmaları oldukça zorlaştıran bir durum. Bir diğer ilginç nokta da Tip 3-B olarak adlandırılan sistemin DNA yerine RNA’yı hedef alması ve parçalaması.
Elbette burada akla gelen en önemli sorulardan biri şu ki nasıl oluyor da bu sistemler kendi DNA’larını parçalamıyor? Sonuçta virüsün DNA’sı ile bu DNA’dan elde edilen aralık geni birbirlerinin aynısı. Bu durumda oluşturulan crRNP hücrenin kendi aralık genini de bir yabancı DNA gibi algılayıp ve parçalamaz mı?
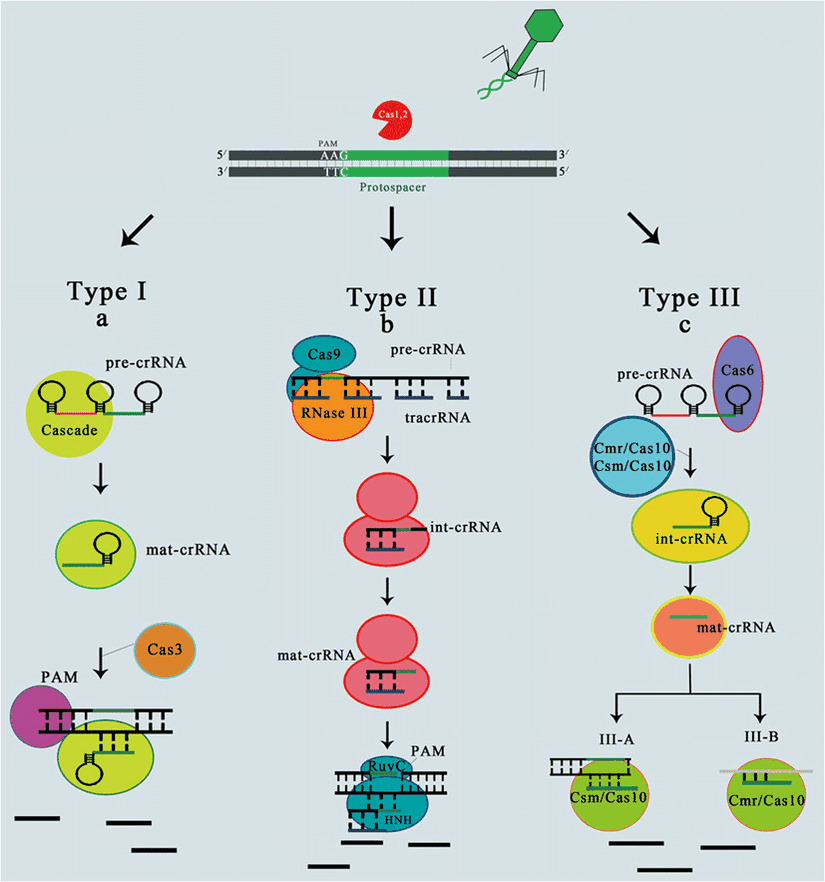
İşte burada, daha önce bahsettiğimiz ve bir bağışıklık sisteminin temeli olan ben ve diğerleri ayrımını yapabilme yeteneği işin içine giriyor. Tip 1 ve 2 sistemlerde PAM (Protospacer Adjacent Motifs) olarak adlandırılan bir DNA dizisi, crRNP’lerin DNA parçalama aktivitesini tetikliyor. PAM dizisinin özelliği, ön-aralık dizisinden (yani işgalci DNA’nın crRNP tarafından tanınan parçası) hemen önce gelmesidir. İkinci bir özelliği ise bariz bir şekilde CRISPR lokusundaki tekrar dizilerinden farklı olmasıdır. Bunu gözünüzde canlandırmaya çalışırsanız bu hücrenin nasıl ben ve diğerleri ayrımını yaptığını fark edeceksiniz. Hücrenin kendi DNA’sında bir tekrar dizisi ve hemen ardından gelen aralık dizisi var. Yabancı DNA’da ise PAM dizisi ve hemen ardından gelen ön-aralık dizisi var (terimler aklınızı karıştırmasın, ön-aralık dizisi ile aralık dizisi birbirinin aynısıdır). PAM dizisine bağlanmak da crRNP’lerin nükleaz aktivitesini tetiklerken tekrar dizisine bağlanmak herhangi bir etki yaratmıyor. Tip 3 sistemlerde ise durum biraz farklı. Bu sistemlerde PAM motifleri kullanılmamakta fakat tekrar dizisine bağlanmak crRNP’nin inaktif hale gelmesine sebep olmaktadır.
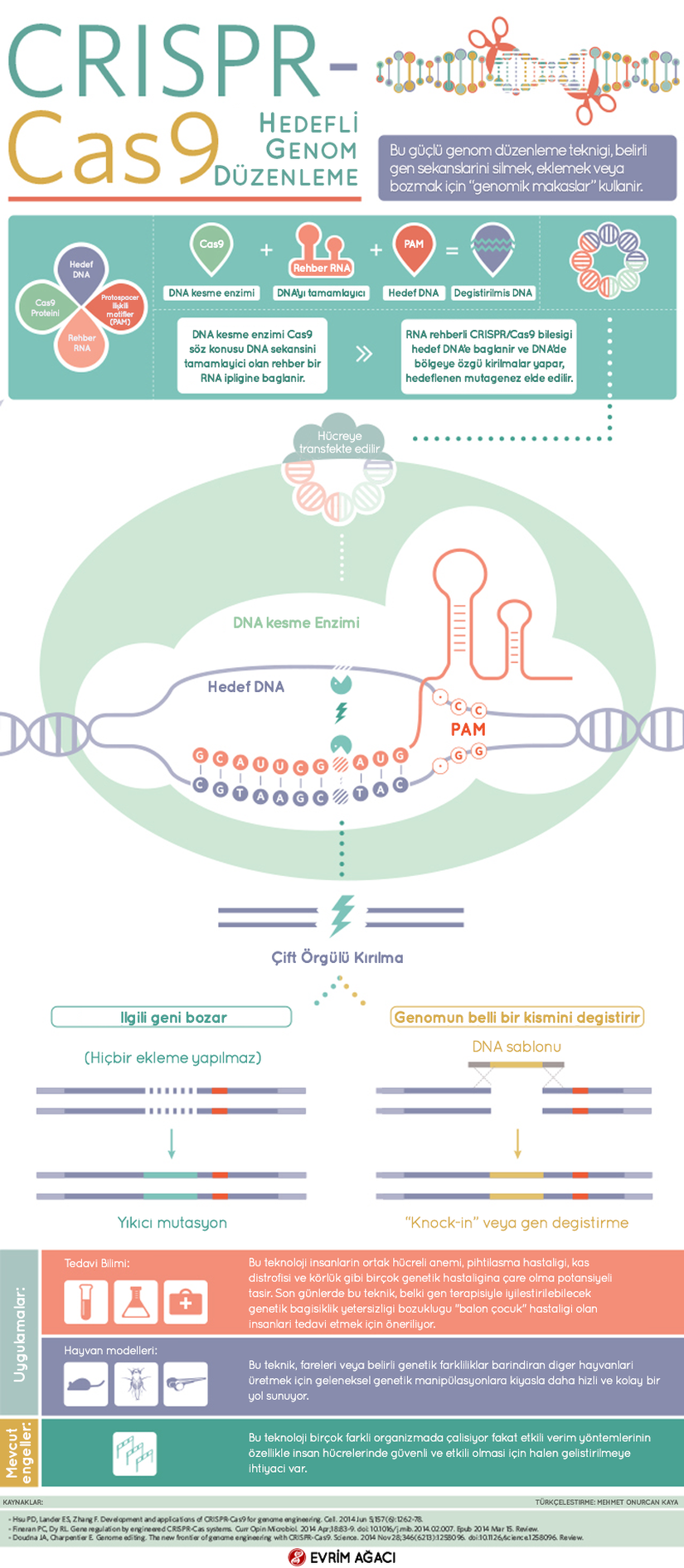
Moleküler biyoloji ve özellikle genetik mühendislik tekniklerine aşina olan okurlar belki de CRISPR sisteminin sağlayabileceği avantajı fark etmiştir bile. Bunu çok daha önceden fark eden Dr. Jennifer Doudna ve ekibi 2012 yılında yayınladıkları bir dizi makale ile bu sistemler üzerinden geliştirdikleri tekniği nasıl genetik mühendisliğinde kullanabileceklerini gösterdiler. İşin güzelliği ise insanı hayrete düşürecek basitliğinde yatıyor. CRISPR sisteminin özelliği belirli bir DNA dizisi üzerinde işlemesidir. Bu da demektir ki herhangi bir DNA’yı yüksek hassaslıkta ve doğrulukta kesebilmemiz için bize gereken tek şey o DNA’nın baz dizisi ve hücre içinde crRNP oluşturabilecek, aktif bir Cas nükleaz proteini. DNA’nın baz dizisine karşılık gelen bir crRNA oluşturuyoruz, bu crRNAyı Cas proteini ile birleştiriyoruz ve hücrenin içine salıyoruz. Bundan sonra tek yapmamız gereken oluşturduğumuz crRNP kompleksinin gidip DNA’yı bizim belirlediğimiz yerden kesmesini beklemek. Bu sayede doğuştan gelen genetik hastalıklardan kansere ve AIDS’e kadar birçok hastalığın tedavisinde kullanılabilecek bir yol açmış oluyoruz.
Birçok araştırmacı tarafından “insanın ağzını açık bırakacak” bir teknik olarak tanımlanan bu teknik şu zamana kadar insan kök hücreleri dâhil birçok canlıda denendi ve oldukça olumlu sonuçlar aldı. Hatta Science dergisi 2013 yılının en önemli bilimsel gelişmelerinden biri olarak bu tekniğin geliştirilmesini seçti. Elbette henüz tekniğin optimize edilmesi adına çok çalışmalar yapılmalı ancak yine de bu çok daha başarılı tedavilerin yakın olduğunu hissetmemizi engellemiyor.
Yazının sonunda Carl Sagan’ın beni çok etkileyen bir örneğinden bahsetmek istiyorum. Karanlık Bir Dünya’da Bilimin Mum Işığı kitabını okuyanlar aşinadır, bugünkü bilgi teknolojimizin ve paylaşımının temelini oluşturan, cep telefonlarımızdan uzay teleskoplarına kadar birçok aletin çalışmasına olanak tanıyan elektromanyetik dalgalar Maxwell’in çalışmaları ile çok daha açık bir şekilde anlaşılmıştır. Fakat Maxwell’in elektromanyetik dalgalar üzerine çalışırken bir cep telefonu düşlediği ile ilgili hiçbir kanıtımız yok. Lafın özü, temel bilim çalışmalarının bize ne gibi olanaklar sağlayacağını her zaman önceden kestiremeyebiliriz. Hazırlıklı olalım ki 10 yıl önce arkelerin edinilmiş bağışıklık sistemi üzerine çalışan ve belki de önemsenmeyen bir bilim insanı 10 yıl sonra birçok genetik hastalığa çare olabilecek bir teknik ile çıkageldiğinde şaşırmayalım.
Genetiği Değiştirilmiş Bebekler ve İnsanlar!
CRISPR yöntemi oldukça gelişmiş olsa da, uzunluk gibi basit bir kavramın bile 180’den fazla genden etkilendiği gerçeği ve genlerin birbirleri arasındaki iletişimi tam kavrayamamamız, rehber virüsün daima yerini bulamaması gibi etmenler ile deyimin tam anlamıyla “kaş yaparken göz çıkarmak” oldukça mümkün, insanda hata marjininin oldukça dar olması da bir başka olumsuz etmen.
Farelerde ve maymunlarda test edilen yöntem, birçok genetik hastalık tedavisi konusunda umut vaadediyor. Farelerde güç, hız ve zeka gibi kavramlar ile oynayabilmekteyiz. “Schwarzenegger”, IGF-1 proteinini üreten bir gen enjeksiyonuyla %40 kas artışı yaşadı. Hız konusunda, yağ yakıcı bir protein kodlayan DNA enjekte edilmiş fareler, normal farelere göre iki kat mesafe katedebiliyorlar ve daha hızlılar. “Doogie”, hipokampüs reseptörünü uyaran NR2B gen enjeksiyonu sonucunda hafıza ve öğrenme kabiliyetinde gelişme gösterdi.

İnsanlarda da test edilmesi gündemde; fakat yöntemin sonuçlarının öngörülemez olması, maymunlarda %20 - %30 başarı oranına sahip olması şimdilik insanlı deneyler için yöntemin yeterince sağlıklı olmadığını gösteriyor. Buna rağmen 2015'te Çin’de ilk defa insan embriyolarındaki β-thalassaemia isimli ölümcül olabilen kan hastalığına neden olan genler değiştirilerek, insanlarda genetik manipulasyon konusunda kritik bir adım atıldı. 2016 yılında ise İngiltere "genetiği değiştirilmiş bebeklere" izin verme yolunda ilk büyük adımları attı.
Henüz kendi özelliklerimizi geliştiremesek de CRISPR/gen terapisi, genetik hastalıkların ve Huntington, Tay-Sachs gibi mutasyon sebebiyle oluşan hastalıkların önüne geçmemizi sağlayabilir.
CRISPR-Cas9 genetik temeli olan çok sayıda tıbbi hastalığın (kanser, hepatit B, talesemi, lösemi, orak hücreli anemi ve hatta yüksek kolesterol) tedavisinde kullanılmak için bir umut vaat ediyor. Yeni yayımlanan çalışmalar genetik temelli hastalıkların tedavisinin mümkün olduğunu kanıtlar nitelikte. Önerilen uygulamaların çoğu somatik hücrelerin genomlarının düzenlenmesi ile ilgili olsa da, üreme hücrelerinin düzenlenme potansiyeline ilişkin etik tartışması sürüyor. Çünkü üreme hücreleri üzerinde yapılacak değişiklikler nesilden nesile kalıtımsal olarak aktarılacağı için olayın ahlaki bir boyutu var. Üreme hücreleri üzerinde gen düzenleme yapmak, şu anda dünyanın pek çok ülkesinde yasa dışıdır.
Kanser Tedavisi
CRISPR gen tedavisi ile kanserlerin tedavi edilebileceği öngörülmektedir. Nitekim ki 2019 yılında Çin’de yürütülen ilk ve en gelişmiş CRISPR klinik deneylerinden biri, yemek borusu kanseri olan hastaları tedavi etmek için gen düzenleme aracının potansiyelini test ediyor.
Hangzhou Kanser Hastanesinde test edilmekte olan tedavi, hastadan bağışıklık T hücrelerinin alınmasıyla başlar. CRISPR kullanılarak hücreler, PD-1 (kanser ve tümör hücrelerinde bulunan immün sistemi baskılamada önemli rol oynayan bir hücre zarı proteini) adı verilen bir proteini kodlayan geni çıkarmak için modifiye edilir - bazı tümörler, bağışıklık hücresinin yüzeyindeki bu proteine bağlanabilir ve onlara saldırmamalarını söyler. Değiştirilen hücreler daha sonra kanser hücrelerine saldırmak için daha yüksek kapasiteye sahip hastaya yeniden infüze edilir.
Şu ana kadar Çin'de farklı kanser türlerine sahip en az 86 kişi CRISPR ile tedavi edildi. ABD'de, Nisan 2018'da tedavi edilen ilk hastalarla yapılan başka bir CRISPR denemesi de kanseri hedefliyor. Pennsylvania Üniversitesi'ndeki bilim insanları, PD-1'i çıkarmak ve ayrıca tümörleri bulup onlara saldırmak için bağışıklık hücrelerinin yüzeyindeki bir molekülü değiştirmek için CRISPR kullanıyor.
Kan Hastalıklarının Tedavisi
Avrupa ve ABD’de birinci CRISPR denemesi 2018 şubat ayında akdeniz anemisi ve orak hücre hastalığında (kandaki oksijen taşınmasını engelleyen iki kan hastalığı) olmuştur. Tedavi hastadan kemik iliği kök hücrelerinin alınması ve CRISPR teknolojisinin, oksijeni yetişkin formundan çok daha iyi bağlayan oksijen taşıyan proteinin doğal bir formu olan fetal hemoglobin üretmesini sağlamaktan ibarettir. Hemofili de CRISPR teknolojisinin üstesinden gelebileceği başka bir genetik hastalıktır.
HIV Tedavisi
CRISPR teknolojisinin potansiyel klinik uygulamalarından biriside, HIV gibi bulaşıcı hastalıkların tedavi edilmektir. Antiretroviral terapi HIV için etkili bir tedavi sağlasa da, virüsün konakçı genomuna kalıcı entegrasyonu nedeniyle şu anda hiçbir tedavi mevcut değildir. HIV virüsü AIDS’e neden olur ve CRISPR’ın burada kullanımı şu şekillerde olabilir.
HIV virüsünün DNA'sını bağışıklık hücrelerinin DNA'sındaki saklandığı yerden çıkarmak için CRISPR kullanılıyor . Bu yaklaşım, virüse gizli, inaktif haliyle saldırmak için kullanılabilir, bu da çoğu tedavinin virüsten tamamen kurtulmasını imkansız kılar.
Başka bir yaklaşım bizi HIV enfeksiyonlarına karşı dirençli hale getirebilir. Bazı bireyler, HIV'in hücreleri enfekte etmek için giriş noktası olarak kullandığı bağışıklık hücrelerinin yüzeyindeki bir proteini kodlayan CCR5 olarak bilinen bir gendeki bir mutasyon sayesinde HIV'e karşı doğal bir dirençle doğar. Mutasyon, proteinin yapısını değiştirir, böylece virüs artık ona bağlanamaz. Bu yaklaşım, geçen yıl Çin'de çok tartışmalı bir davada kullanıldı. CRISPR-Cas9, insan embriyolarını HIV enfeksiyonlarına dirençli hale getirmek için düzenlemek için kullanıldı. Bunun ileride belki daha fazla bozukluğa neden olmayacağına dair herhangi bir kanıtın olmaması bilimsel çevrelerde öfkeye neden oldu. Genel fikir birliği, bu yaklaşımın insanlarda kullanılabilmesi için daha fazla araştırmaya ihtiyaç olduğu gibi görünüyor.
Kistik Fibroz Tedavisi
Kistik fibroz (KF), doğumdan itibaren solunum sistemi, sindirim sistemi ve üreme sistemininde yer alan mukus ve ter bezlerini etkileyen kalıtsal bir hastalıktır. Kistik fibroz özellikle, akciğerler, pankreas, karaciğer, bağırsaklar, sinüsler ve cinsel organların işlevini önemli derecede etkilemektedir. Bu hastalığa sahip bir kişinin yaşam beklentisi 40 yıl civarıdır. CRISPR teknolojisi, CFTR adı verilen bir gende bulunan kistik fibroza neden olan mutasyonları düzenleyerek sorunun kaynağına ulaşmamıza yardımcı olabilir.
Araştırmacılar, CRISPR'ı kistik fibrozlu hastalardan elde edilen insan akciğer hücrelerinde kullanmanın ve hastalığın arkasındaki en yaygın mutasyonu düzeltmenin mümkün olduğunu kanıtladılar. Bir sonraki adım ise bunu insanlar üzerinde denemek.
Bununla birlikte, kistik fibroz, CFTR genindeki çok sayıda farklı mutasyondan kaynaklanabilir, bu da farklı genetik kusurlar için farklı CRISPR tedavilerinin geliştirilmesi gerektiği anlamına gelir.
Körlük Tedavisi
CRISPR, genetik körlüğü tedavi etmek için harika bir adaydır. Birçok kalıtsal körlük biçimi, belirli bir mutasyondan kaynaklanır, bu da CRISPR-Cas9'a tek bir geni hedeflemesi ve değiştirmesi talimatını vermeyi kolaylaştırır. Ek olarak, göz vücudun immün sisteminin ayrıcalıklı bir parçasıdır, yani burada bağışıklık sisteminin aktivitesi sınırlıdır. Bu, CRISPR'ın kendisine karşı oluşabilecek bağışıklık reaksiyonlarına karşı avantajlı olduğunu göstermektedir.
Editas Medicine (CRISPR – Cas9 gen düzenleme teknolojisine dayalı tedaviler geliştirmeyi amaçlayan Cambridge, Massachusetts merkezli, keşif aşamasındaki bir ilaç şirketidir.), kalıtsal çocukluk körlüğünün en yaygın nedeni olan ve tedavisi olmayan Leber konjenital amorozu için bir CRISPR tedavisi üzerinde çalışıyor. Şirket, çocukların görüşlerini tamamen kaybetmeden önce ışığa duyarlı hücrelerin işlevini eski haline getirmek için CRISPR kullanarak hastalığın arkasındaki en sık mutasyonu hedeflemeyi hedefliyor.
Musküler Distrofi Tedavisi
Duchenne'in kas distrofisine, kasların kasılması için gerekli bir proteini kodlayan DMD genindeki mutasyonlar neden olur. Duchenne Musküler Distrofi (DMD), kas hastalıkları arasında en sık karşılaşılan hastalıktır. Sadece erkek çocuklarda görülen bir hastalıktır. Bu hastalığa neden olan protein eksikliğinde kaslar giderek zayıflar, kas dokusunun yerini yağ dokusu alır.
Farelerde yapılan araştırmalar, CRISPR teknolojisinin hastalığın arkasındaki çoklu genetik mutasyonları düzeltmek için kullanılabileceğini göstermiştir. 2018 yılında, ABD'deki bir grup araştırmacı, her bir mutasyonu ayrı ayrı sabitlemek yerine, CRISPR'yi kullanarak bu kas hastalığına neden olan tahmini 3.000 farklı mutasyonun çoğunu kapsayan 12 stratejik ‘’mutasyon sıcak noktasını’’ kesmek için kolları sıvadı. Bu yaklaşımı daha da geliştirmek için Exonics Therapeutics adlı bir şirket kuruldu.
Huntington Hastalığı Tedavisi
Huntington hastalığı, hastaların davranışsal bozukluk, zihinsel yıkım ve kontrol edilemeyen hareketler yaşadığı nadir, ilerleyici bir genetik bozukluktur. Huntington hastalığı beyinde striatumun yavaş yavaş atrofiye uğradığı kalıtsal bir hastalıktır. Hastalığa, Huntingtin geni içindeki belirli bir DNA sekansının anormal bir şekilde tekrarlanması neden olur. Kopya sayısı ne kadar yüksekse, hastalık o kadar erken kendini gösterir.
CRISPR'ın beyindeki herhangi bir hedef dışı etkisinin çok tehlikeli sonuçları olabileceğinden, Huntington'ları tedavi etmek zor olabilir. Riski azaltmak için bilim insanları, gen düzenleme aracını daha güvenli hale getirmenin yollarını arıyorlar.
Embriyonik Kök Hücre ve Transgenik Hayvanlar
CRISPR-Cas sistemleri, genetik olarak modifiye edilmiş farelerin üretimi için murin embriyonik kök hücrelerinde bir veya daha fazla genetik değişikliği hızlı ve verimli bir şekilde yapılandırmak için kullanılabilir. Primat tek hücreli embriyoları genetik olarak modifiye etmek için benzer bir yaklaşım kullanılmıştır.
CRISPR-Cas9 Riskli mi?
Biyolojik sistemlerde genom modifikasyonu ve fonksiyonel düzenlemede etkili bir şekilde yararlı olmasına rağmen, CRISPR / Cas9 sistemleri aynı zamanda çeşitli zorluklarla da karşılaşmıştır. Bunların arasında hedef dışı etki en başta gelen zorluktur.
Tüm önlemleri aldınız ve CRISPR kılavuz RNA'larınızı spesifik olacak ve yalnızca ilgilendiğiniz genetik bölgeyi hedef alacak şekilde tasarladınız. Kılavuz RNA dizisinin genomda benzersiz olduğunu iki kez kontrol ettiniz. Cas9 yalnızca belirli bir bölgeyi kesmeli, değil mi? Yanlış.
Teoride, CRISPR-Cas9 sistemi inanılmaz derecede spesifiktir, pratikte değildir. Genomun başka bir yerinde hedef dışı modifikasyonlar olarak bilinen mutasyonlar yaratabilir. Hedef dışı etkiler rastgeledir ve diğer genleri veya genomun bölgelerini etkileyebilir. Son birkaç yılda, araştırmacılar sgRNA’yı optimize ederek veya Cas9'un PAM yapısı gibi protein yapısını yapay olarak değiştirerek iyileştirmeler yapmaya çalıştılar . Ek olarak, Cas9'un çekirdekte aktif olduğu süreyi sınırlayarak istenmeyen hedef dışı etkilerden kaçınmak için yararlı bir Cas9 kapatma anahtarı olmayı vaat eden anti-CRISPR proteinlerine yönelik araştırmalar vardır. Ancak, hedef dışı herhangi bir etkiniz olmadığından asla% 100 emin olamazsınız. Sonuçlar potansiyel olarak felaket olabilir.
Riski Nasıl Azaltabiliriz?
Bilim insanları CRISPR-Cas9 sisteminin hatasız bağlanmasını ve genomda doğru yeri kesmesini garantileyecek iki yol üzerinde çalışıyor:
- Genomun DNA dizilimi ve Cas9-rehber RNA kompleksinin farklı versiyonlarının “hedef dışı” davranışları hakkındaki bilgiler kullanarak daha ayrıntılı rehber RNA’lar yapmak.
- DNA’nın iki ipliğini birden değil de, sadece tek ipliğini kesecek Cas9 enzimi kullanmak. Bu da aynı anda iki rehber RNA ve iki Cas9 enzimi kullanmak ve böylece yanlış yerde kesim yapılma olasılığını düşürmek anlamına geliyor.
DNA’mıza geçen ve hastalığa neden olan bir hatayı düzeltmek isteyebiliriz. Veya bazı durumlarda bitkilerin, hayvanların ve hatta insanların genetik kodlarını geliştirmek isteyebiliriz. Yani tek ihtiyacımız olan dev bir mikroskop ve küçük bir makas. Ve CRISPR-Cas9 yönteminde kullanılan da özünde bu...
Cas9'un hücrelere veya dokuya teslim verimliliği, CRISPR aracılı genom düzenlemesinin başarılı olmasını engelleyen başka bir sorundur. Düzenleme verimliliği birçok faktörden etkilenebilir ve herhangi bir genom düzenleme deneyini ciddi bir şekilde etkileyebilir. Bunu önlemenin yolları var. En yaygın yöntem, Cas9 ekspresyon vektörünüze seçim işaretlerini dahil etmek ve başarıyla transfekte edilmiş hücre popülasyonunu seçmektir. Bununla birlikte, bu yaklaşımın potansiyel olarak ölümcül olabilecek iki ana uyarısı vardır:
- Antibiyotiklerle toksik seleksiyon varlığında hücreleriniz artık "normal" davranmayabilir.
- Hücreleriniz kültürde kolayca bölünmez veya genişlemezse, hücrelerinizin bir alt popülasyonunun seçilmesi, çalışmak zorunda olduğunuz hücre sayısını sınırlayabilir.
Öyleyse Sadece İstenmeyen Bir Geni Koparıp ve Yerine İyi Bir Gen Koyabilir Miyiz?
Genetik hastalığa neden olan nokta mutasyonu tedavisi için DNA’daki o mutasyonlu yeri kesmek hasta için hiçbir fayda sağlamaz. Çünkü mutasyonlu genin fonksiyonu yeniden yüklenmelidir. CRISPR-Cas9’la birlikte hücreye verilen sağlıklı gen, mutasyonlu hücrede bulunan DNA onarım mekanizmasını kullanarak yerleşir ve hücrenin normal fonksiyona sahip olmasını sağlar.
Yakın zamanda yayımlanan makaleye göre, süreçte yer alan olayların sırasını daha iyi anlamak için araştırmacılar Cas9 enzimini görüntüleyen cryo-EM teknolojisini buldular. British Columbia Üniversitesi ve Frederick Ulusal Kanser Araştırma Laboratuvarı araştırmacısı Dr. Sriram Subramaniam bunu şöyle açıklıyor:
Cas9’un DNA iplikçiklerini kesmek ve düzenlemek için gerçekten nasıl çalıştığını çok yüksek düzeyde görebilmek heyecan verici. Bu görüntüler, gen-kurgu sürecinin verimliliğini artırmak için bize paha biçilemez bilgi sağlıyor. Böylece gelecekte hastalığa neden olan DNA mutasyonlarını daha hızlı ve hassas bir şekilde düzeltebiliriz.
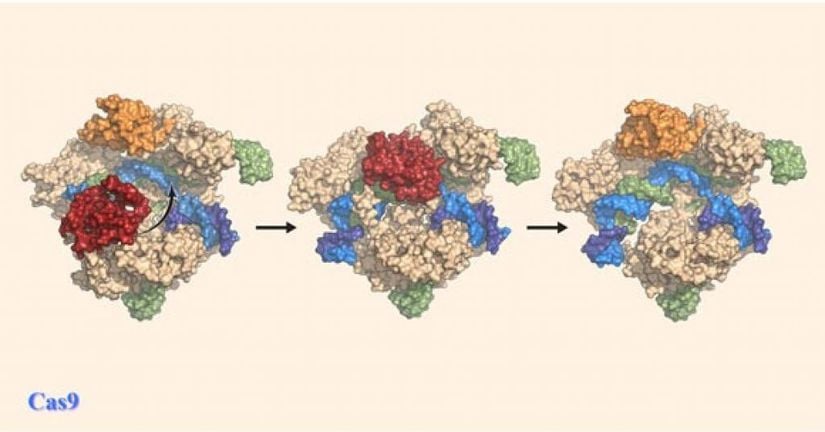
Chicago’daki Illinois Üniversitesinden Dr. Miljan Simonoviç şöyle diyor:
Daha iyi gen düzenleme araçlarının geliştirilmesini önleyen en büyük engellerden biri, DNA’yı kesen Cas9'un hiçbir görüntüsüne sahip olmamamızdır. Fakat şimdi daha net bir resme sahibiz ve enzimin reaksiyon sırasında nasıl hareket ettiğini görebiliyoruz. Bunun da gen modifikasyonunu gözlemlemek için çok önemli olduğunu düşünüyoruz.
İnsan Genomu Düzenleme Çalışmalarında Araştırma Etiğinin Değerlendirilmesi
CRISPR-Cas9 teknolojisi kullanılarak insan eşey hücre öncülleri (human germline) düzenlemelerinin gelişmesi ile birlikte embriyolar üzerinde araştırmalar yapılması açısından bazı acil etik hususlar öne çıkıyor.
20 Eylül 2017 tarihinde Nature'da, insan embriyosu kullanılarak DNA üzerinde yapılan gen düzenleme ve değiştirme çalışmaları sonucunda araştırmaların deney sonuçları yayınlandı. Francis Crick Enstitüsünden Kathy Niakan ve çalışma arkadaşları, CRISPR-Cas9 teknolojisini kullanarak OCT4 adı verilen gen içerisindeki mutasyonları gösterdiler. Döllenmiş bir yumurta bölünüp çoğalırken hücre içerisindeki genin hücre kaderini nasıl yönlendirdiğini yine aynı teknolojiyi kullanarak gösterdiler.
Araştırma insan biyolojisi açısından temel bir soruyu ele alıyor, fakat erken gelişim süreçlerini anlamak gelecekteki tüp bebek işlemlerinde embriyoların kültür durumlarının düzeltilmesinde yardımcı olabilir. Ayrıca gen düzenleme tekniğini destekleyen mekanizmalar hakkında da önemli bilgiler sunabilir. Tüp bebek tedavisi gören çiftlerin bağışladığı embriyoların laboratuvar ortamında sadece birkaç gün gelişmesine izin verildi.
Nature, Ağustos 2017’de de, CRISPR-Cas9 teknolojisi kullanılarak embriyo içerisinde meydana gelen spesifik gen mutasyonlarının gen düzenleme ile nasıl düzeltilebileceği konusunda bir araştırma makalesi yayınladı. Bu deneyler Oregon Sağlık ve Bilim Üniversitesinden Shoukhrat Mitalipov ve çalışma arkadaşları tarafından IVF kliniklerinden embriyo alınmadan yapıldı. Bunun yerine mutant genler taşıyan bir erkek donörün spermi laboratuvar ortamında başka bir donörün yumurtası ile döllenerek embriyo oluşturuldu.
Bu çalışmaların yayınlanması, tüm katılımcıların konuyu ayrıntılı olarak değerlendirmesi ve ayrıca bu tip araştırmalara nasıl yön verilmesi gerektiğini tartışması açısından iyi bir zaman gibi gözüküyor.
Etik Açıdan Ortak Görüş
CRISPR-Cas9 teknolojisi dikkatle takip edilmesi gereken etkili bir genom düzenleme yöntemidir, çünkü bilim insanlarının insan eşey hücre öncüllerini kalıcı olarak değiştirmesi gibi bir durum söz konusu olabilir. Alanında uzman bilim insanları, etik açıdan itirazlarını ayrıntılı olarak listeleyip insan embriyosunda uygulanacak gen düzenleme araştırmalarının bundan sonra nasıl yürütülmesi gerektiği hakkındaki tavsiyelerini açıkladılar. Bu çabalarını disiplinlerarası etik konsorsiyuma temellendiren Hinxton Topluluğu ve aynı şekilde ayrı olarak çaba gösteren Amerikan Bilim, Mühendislik ve Tıp Akademileri, Uluslararası Kök Hücre Araştırmaları Topluluğu gibi kuruluşlar temel biyoloji dahilinde insan eşey hücre öncülleri düzenleme araştırmalarının bilimsel amaçlara uygun olacak şekilde kullanılabileceği konusunda fikir verdiler.
Ayrıca gen düzenlemenin klinik bir araç olarak kullanılabilmesi için güvenlik, doğruluk ve uygulanabilirlik açısından temel araştırma yöntemleriyle titiz bir şekilde incelenmesi gerektiğini söylediler. Bu nedenle ancak güçlü bir araştırma altyapısı oluşturulduktan sonra ve ancak o zaman da alternatifler dikkatli bir şekilde incelenip daha fazla toplumsal tartışma yapıldıktan sonra kabul edilebilir bulunan vakalar için klinik uygulamalar düşünülebilir.
Nature'da yayınlanan araştırmalar bazı temel bilimsel sorulara cevap vermeyi amaçlıyor. Ve tabii ki etik ilkelere bağlı kalarak, araştırmaların başlangıcı, uygulanması ve hakem incelemesi (ilkelerimizde belirtildiği gibi) esnasında sıkı ve eksiksiz bir etik değerlendirme ile kontrol edildiler. Araştırmaların her ikisi de embriyo, sperm ve yumurta donörlerinin tam rızası ve etik onayını almışlardı ve ilgili makamlarca yetkilendirilmişlerdi.
Bu çalışmalar birkaç nokta açısından değerlidir. İnsan embriyosu biyolojisinin ve bu bağlamda gen düzenleme sisteminin muhtemel mekanizmalarının anlaşılmasında önemli katkılar sağlıyorlar. Ayrıca önemli teknik ve etik sorunları öne çıkararak bu alanda gelecek araştırmaları değerlendirip planlayan araştırmacılara, kaynak sağlayıcılara, dergilere ve denetleyicilere (regulator) bilgi sağlamış oluyorlar.
Özellikle eşey hücre öncüllerini düzenlemenin farklı yönlerini araştıran insan embriyo projeleri için uygun embriyo tipi ve sayısının doğru bir şekilde değerlendirilmesinin önemini gösteriyorlar.
IVF çalışmalarından arta kalarak bağışlanan embriyoların kullanılması, laboratuvar ortamında döllenen embriyoların kullanılmasına nazaran bazı araştırma sorularına çözüm bulmak için daha iyi bir yol olabilir. Bağışlanan embriyodaki doğal çeşitlilik, CRISPR Cas-9 düzenlemesi sırasında oluşabilecek istenmeyen “hedef dışı” genetik değişiklikler gibi sorunları kontrol etmek için daha titiz ve gerçekçi bir test imkanı sunabilir. Fakat şu an için spesifik mutasyonların hedef odaklı olarak düzeltilmesi, donörlerden alınan o mutasyonlara sahip üreme hücrelerinin laboratuvar ortamında döllenmesiyle devam edecek gibi görünüyor.

Her iki durumda da, Nature, her iki makalenin de metotlar bölümünde belirtildiği gibi, bütün donörlerin kendilerinden alınan örneklerle yapılacak araştırmaların tüm detayları hakkında bilgilendirilmesi taraftarıdır.
Araştırmacılar, bağış yapmanın hassas yapısına bağlı kalarak, kullanılacak embriyoların sayısını belirlemede etik ve bilimsel hususları dengeli bir şekilde göz önünde bulundurduklarını göstermelidirler. Araştırmacılar bu değerli materyali minimum seviyede kullanarak, yaptıkları deney ve araştırmaların güçlü ve sağlam bilimsel cevaplar vermelerini sağlamak zorundadırlar. Bu, araştırmacıların ilk olarak çalışmalarında insan pluripotent kök hücreleri veya fare embriyolarını kullanarak deney koşullarını optimize etmeleri anlamına gelebilir ki yayınlanan her iki çalışmada da bu yol izlenmiştir. Dergiler, inceleme ekibindekiler ve editörler hakem incelemesi sırasında ortaya çıkan soruların insan embriyolarından başka sistemler kullanılarak cevaplanıp cevaplanamayacağını göz önünde bulundurmalıdırlar.
Araştırma camiasının düşünmesi gereken bir başka konu da hipotezin embriyolar üzerinde test edilmesinden önce ön çalışmaların hakem incelemesinden geçirilip yayına uygun olup olmadığının düşünülmesi olabilir. Bağımsız olarak yapılan bu hakem incelemesi ile denetleyicilerin incelemesi paralel olarak yürütülebilir, ve böylece deneylerin sınırları ve embriyoların menşei hakkında alınacak kararlara bilgi sağlanabilir.
Her çalışmada yerine getirilmesi gereken belirli şartlar farklı olabilir, fakat mümkün olduğunca en erken sürede bu şartları değerlendirmek için güçlü bir temel yapının oluşturulması, onların en iyi şekilde yapıldıklarından emin olmanın en doğru yolu olarak görünüyor. Denetleyiciler, kaynak sağlayıcılar, bilim insanları ve editörler eşey hücre öncüllerini düzenleme sistemini daha ileriye taşıyacak yolun detaylarını belirlemek için birlikte çalışmaya devam etmelidirler. Ancak bu yolu izleyerek elimizdeki değerli kaynak ve araçları en doğru şekilde kullanabiliriz.
İçeriklerimizin bilimsel gerçekleri doğru bir şekilde yansıtması için en üst düzey çabayı gösteriyoruz. Gözünüze doğru gelmeyen bir şey varsa, mümkünse güvenilir kaynaklarınızla birlikte bize ulaşın!
Bu içeriğimizle ilgili bir sorunuz mu var? Buraya tıklayarak sorabilirsiniz.
İçerikle İlgili Sorular
- CRiSPR ile telomer kısalmasını azaltmak yahut engellemek mümkün müdür?
- CRISPR Cas-9 teknolojisi hangi ölçekte kullanılabilir?
- 40
- 20
- 17
- 15
- 15
- 10
- 10
- 2
- 0
- 0
- 0
- 0
- B. Wiedenheft, et al. (2012). Rna-Guided Genetic Silencing Systems In Bacteria And Archaea. Nature, sf: 331-338. | Arşiv Bağlantısı
- J. van der Oost, et al. (2014). Unravelling The Structural And Mechanistic Basis Of Crispr–Cas Systems. Nature Reviews Microbiology, sf: 479-492. | Arşiv Bağlantısı
- S. Connor. Exclusive: 'Jaw-Dropping' Breakthrough Hailed As Landmark In Fight Against Hereditary Diseases As Crispr Technique Heralds Genetic Revolution. (7 Kasım 2013). Alındığı Tarih: 12 Ağustos 2019. Alındığı Yer: The Independent | Arşiv Bağlantısı
- T. Prentice. Health, History And Hard Choices: Funding Dilemmas Funding Dilemmas In A Fast In A Fast--Changing World Changing World. (1 Ağustos 2006). Alındığı Tarih: 12 Ağustos 2019. Alındığı Yer: WHO | Arşiv Bağlantısı
- Wired. Top Scientific Discoveries Of 2013. (18 Aralık 2013). Alındığı Tarih: 12 Ağustos 2019. Alındığı Yer: Wired | Arşiv Bağlantısı
- Nature Editors. Take Stock Of Research Ethics In Human Genome Editing. (20 Eylül 2017). Alındığı Tarih: 12 Ağustos 2019. Alındığı Yer: Nature | Arşiv Bağlantısı
- D. Cyranoski. Dna Editing Of Human Embryos Alarms Scientists. (13 Mart 2015). Alındığı Tarih: 12 Ağustos 2019. Alındığı Yer: Scientific American | Arşiv Bağlantısı
- J. Gallagher. 'Designer Babies' Debate Should Start, Scientists Say. (19 Ocak 2015). Alındığı Tarih: 12 Ağustos 2019. Alındığı Yer: BBC | Arşiv Bağlantısı
- H. Manghwar, et al. (2019). Crispr/Cas System: Recent Advances And Future Prospects For Genome Editing. Trends in Plant Science, sf: 1102-1125. doi: 10.1016/j.tplants.2019.09.006. | Arşiv Bağlantısı
- Bitesize Bio. Crispr-Cas9 Genome Editing: Weighing The Pros And Cons. (23 Eylül 2019). Alındığı Tarih: 27 Ağustos 2020. Alındığı Yer: Bitesize Bio | Arşiv Bağlantısı
- Science News for Students. Explainer: How Crispr Works. (31 Temmuz 2017). Alındığı Tarih: 27 Ağustos 2020. Alındığı Yer: Science News for Students | Arşiv Bağlantısı
- P. D. Hsu, et al. (2014). Development And Applications Of Crispr-Cas9 For Genome Engineering. Cell, sf: 1262. doi: 10.1016/j.cell.2014.05.010. | Arşiv Bağlantısı
- British Society for Gene and Cell Therapy. Crispr/Cas: From Yogurt To Genome Engineering | British Society For Gene And Cell Therapy. (18 Kasım 2015). Alındığı Tarih: 27 Ağustos 2020. Alındığı Yer: British Society for Gene and Cell Therapy | Arşiv Bağlantısı
- M. Redman, et al. (2016). What Is Crispr/Cas9?. Archives of Disease in Childhood - Education and Practice, sf: 213-215. doi: 10.1136/archdischild-2016-310459. | Arşiv Bağlantısı
- C. R. Fernández. 7 Diseases Crispr Technology Could Cure. (23 Temmuz 2019). Alındığı Tarih: 27 Ağustos 2020. Alındığı Yer: Labiotech.eu | Arşiv Bağlantısı
Evrim Ağacı'na her ay sadece 1 kahve ısmarlayarak destek olmak ister misiniz?
Şu iki siteden birini kullanarak şimdi destek olabilirsiniz:
kreosus.com/evrimagaci | patreon.com/evrimagaci
Çıktı Bilgisi: Bu sayfa, Evrim Ağacı yazdırma aracı kullanılarak 25/04/2024 09:09:47 tarihinde oluşturulmuştur. Evrim Ağacı'ndaki içeriklerin tamamı, birden fazla editör tarafından, durmaksızın elden geçirilmekte, güncellenmekte ve geliştirilmektedir. Dolayısıyla bu çıktının alındığı tarihten sonra yapılan güncellemeleri görmek ve bu içeriğin en güncel halini okumak için lütfen şu adrese gidiniz: https://evrimagaci.org/s/407
İçerik Kullanım İzinleri: Evrim Ağacı'ndaki yazılı içerikler orijinallerine hiçbir şekilde dokunulmadığı müddetçe izin alınmaksızın paylaşılabilir, kopyalanabilir, yapıştırılabilir, çoğaltılabilir, basılabilir, dağıtılabilir, yayılabilir, alıntılanabilir. Ancak bu içeriklerin hiçbiri izin alınmaksızın değiştirilemez ve değiştirilmiş halleri Evrim Ağacı'na aitmiş gibi sunulamaz. Benzer şekilde, içeriklerin hiçbiri, söz konusu içeriğin açıkça belirtilmiş yazarlarından ve Evrim Ağacı'ndan başkasına aitmiş gibi sunulamaz. Bu sayfa izin alınmaksızın düzenlenemez, Evrim Ağacı logosu, yazar/editör bilgileri ve içeriğin diğer kısımları izin alınmaksızın değiştirilemez veya kaldırılamaz.


