Ekoloji Araştırmalarında Hangi Moleküler Teknikler ve Genetik Belirteçler Kullanılır?

Ekoloji, ayrılmaz bir şekilde organizmaların evrimsel tarihi ile iç içe geçmiştir. Nesillerin değişim süreci boyunca, organizmalar sürekli olarak bir nesilden diğerine kendinden sonraki nesillerin DNA’sına kaydedilecek genetik bilgi aktarırlar. Moleküler biyologların bu kayıtlara ulaşma becerileri, türlerin kökenlerini ve varoluşlarının ekolojik temellerini daha iyi anlamada modern ekoloji araştırmalarının temel taşı haline geldi.
Bu makalede modern ekologların türlerin oluşumu, çeşitlenmesi ve sürekli değişken, karmaşık çevre şartlarına evrimsel adaptasyonundaki genetik temellerin en derin şekilde anlaşılması için kullandıkları moleküler araçlar ve metotların kısa bir özetini yapacağız.
PCR: Bir Ekoloğun En İyi Arkadaşı
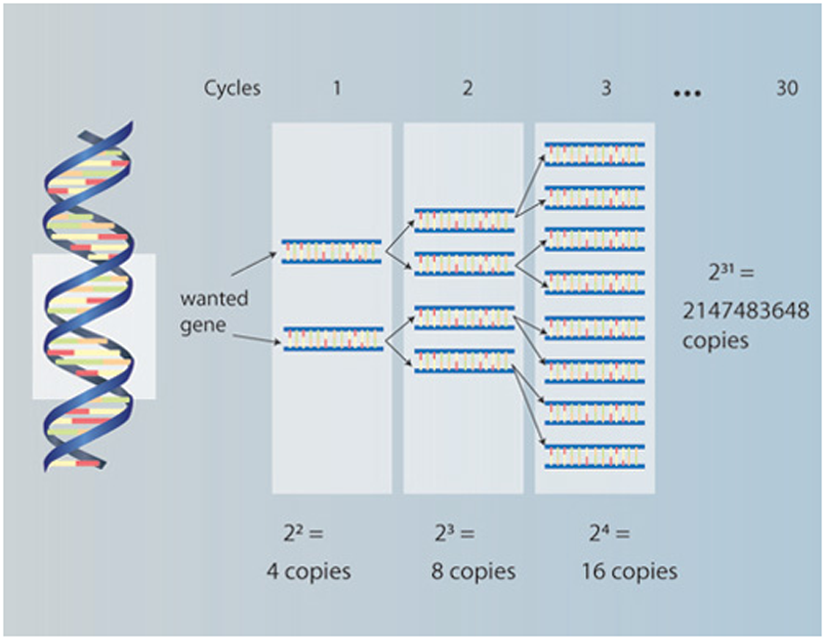
Çoğu moleküler temelli araştırma, belirli bir organizmadan DNA eldesinin (DNA çıkartılmasının) ardından, elde edilen DNA’nın belirli bir bölgesinin polimeraz zincir reaksiyonu aracılığıyla (Polymerase Chain Reaction- PCR) çoğaltılması ile başlar (Şekil 1) . PCR’nin kullanışlığı çok küçük miktarlarda (yaklaşık nanogram düzeyinde) DNA ile yapılabilir olmasında yatıyor. PCR’nin bu özelliği, tıpkı popülasyon genetiği çalışmalarında olduğu gibi, özellikle araştırmacıların büyük miktarda dokuya ulaşmaları zor olduğunda (mesela doğada nadir bulunan bir bitki veya hayvan türü ile çalışma) veya fazla sayıda örneğe ihtiyaç duyulması durumlarında çok işe yarar oluyor.
Bir ekolog şunu sorabilir: “Tek bir türün karşısında uçsuz bucaksız bir çevresel değişim olduğunu düşünürsek, popülasyonlar genetik olarak ne kadar çeşitlidir?" Cevap, çok sayıda popülasyonun farklı örneklerinden DNA elde edip PCR-temelli bir yaklaşımla genetik çeşitliliği incelemekle başlar.
Popülasyonların çok çeşitli coğrafi ve çevresel koşullara yayılmış genetik yapılarındaki değişiklikleri ortaya koyacak tarihsel süreçler hakkında çıkarımlar yapılmasını ancak böyle bir inceleme sağlayabilir. Mesela, bir tür grubunun üyeleri arasındaki evrimsel tarih ve ilişkileri bilinmek istenebilir.
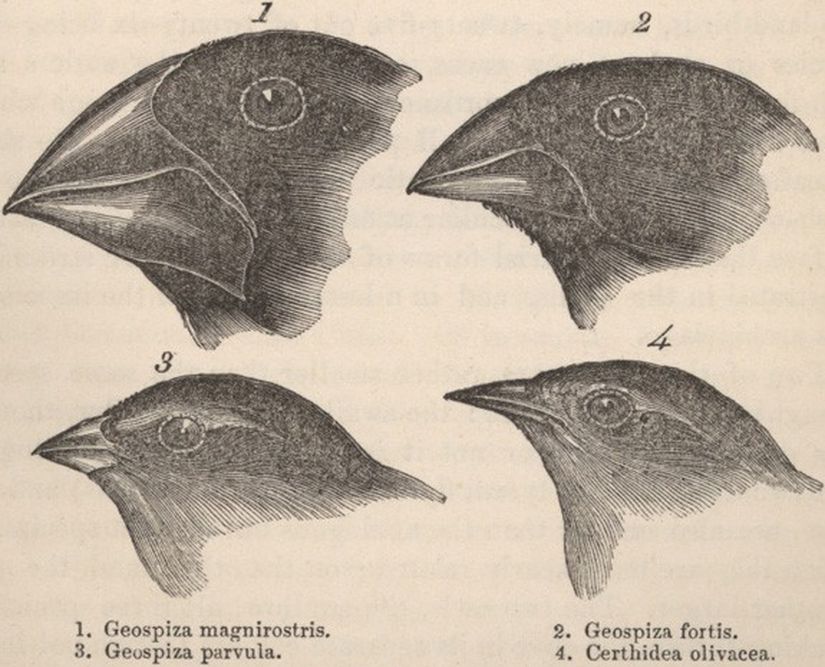
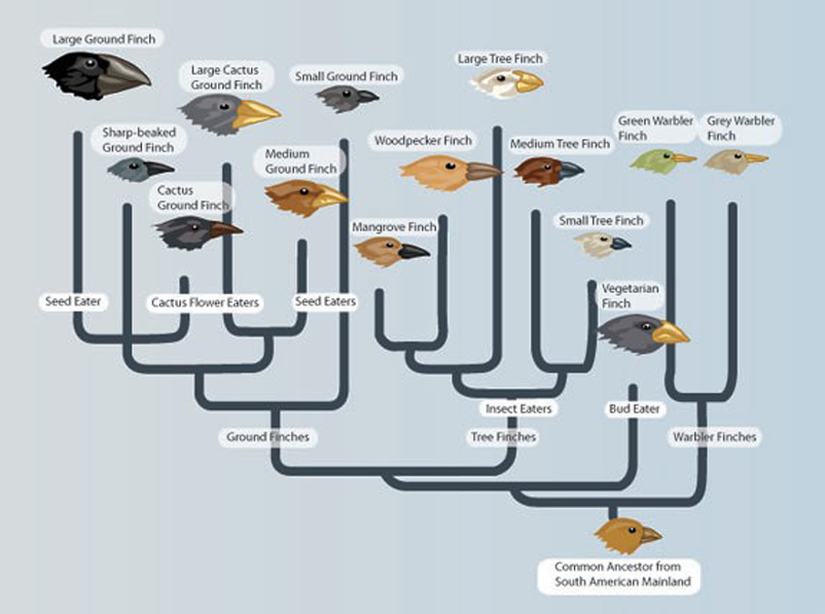
Darwin’in ispinoz kuşlarını düşünün (Şekil 2). Kompleksteki her türün filogenetik tarihini yeniden inşa etme nihai amacıyla, farklı türlerden DNA’ların belirli yerlerindeki kodlayan ve kodlamayan bölgelerini çoğaltmak için PCR kullanılmaktadır. Bu çalışmadan çıkarılacak filogenetik ağaç bize türlerin ne kadar karmaşık olduklarını ve birbirlerine ne kadar yakın ya da uzak olduklarını gösterebilir (Şekil 3). Ve akabinde, bir türün çeşitliliğine katkı sağlayan ekolojik (örn. niş-alan kullanımı) ve davranışsal faktörleri (örn. yiyecek arama) kavramamızı sağlayabilir.
Marker’lar (Belirteçler) ve Metotlar
Moleküler ekolojide kullanılan çok farklı tipte DNA belirteci vardır. Örneğin, mikrosatellitler (MSAT’lar, genellikle insanları kimliklendirmede kullanılan DNA’nın çok tekrarlı ve hızlıca mutasyona uğrayan dizileri), minisatellitler (mikrosatellitlere benzer fakat daha uzun tekrarlı diziler), restriksiyon parça uzunluk polimorfizmleri (RFLP’ler; farklı türler, popülasyonlar, nadiren de insanlarda DNA’yı belirli bölgelerden kesip farklı uzunluklarda parçalar elde edilmesini) ve DNA dizileme verileri (DNA bazlarının benzerlikleri ve farklılıkları, türleri, popülasyonları ve insanları tanımlamak için belirlenmiştir). Bu yöntemlerle elde edilmiş belirteçler farklı yollarla gözle görülür hale getirilir. MSAT’lar ve RFLP’ler agaroz jel elektroforezinden sonra belirgin bantlar şeklinde gözlenir.
DNA dizilerini belirleyen nükleotidler sıklıkla poliakrilamid jeller ve otoradyografi gibi daha yüksek çözünürlüklü yöntemler gerektirir. Bugün bu belirteç tipleri genellikle işaretli primerlerin fluoresan emisyonunu (MSAT’lar için olduğu gibi) veya fluoresan işaretli-DNA’yı algılayan, kemifluoresans ve genetik analiz cihazlarıyla görüntülenir. Belirteçler ve görüntüleme teknikleri asla bunlarla sınırlı değildir ve seçilen teknik çalışmada aranan cevaplara göre belirlenir. Farklı belirteç metotlarının sunduğu farklı türde bilgilerin ışığında, çalışmanın özelinde hangi yöntemin en iyi olacağına karar verilir. Aşağıda moleküler ekoloji çalışmalarında sıklıkla kullanılan üç yöntemi tanımlayacağız.
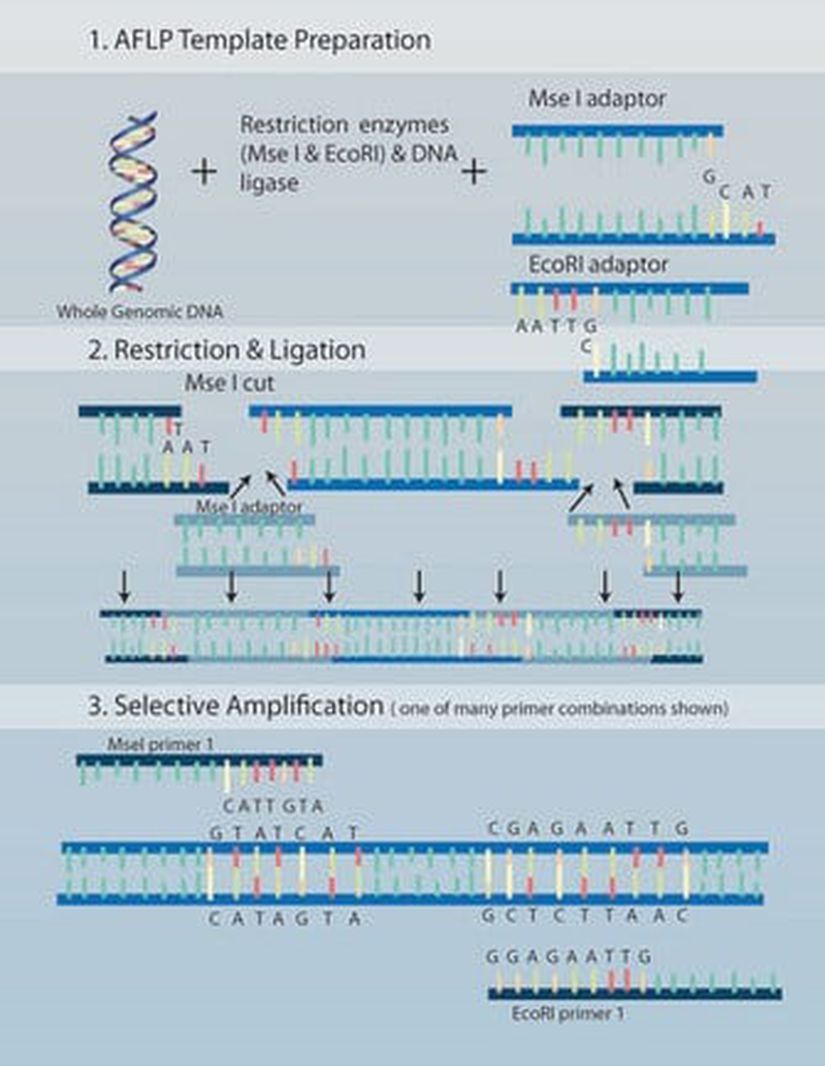
Sundukları bilgilere göre kolayca ayırt edilebilen 3 farklı belirteç sınıfı vardır. Anonim belirteçler, AFLP denilen (Amplified Fragment Length Polymorphisms- çoğaltılmış parça uzunluk polimorfizmleri) bir metotla gözlemlenir (Şekil 4). Bu teknikle, restriksiyon enzimleri ve PCR tekniği birleştirilerek elde edilen birbirinden farklı binlerce DNA parçası sayesinde aynı cinsteki bireylerin tür içi ve türler arası genetik parmak izleri çıkartılabilir. AFLP metodunun avantajı, incelenen organizmanın genom bilgisine ihtiyaç olmamasıdır. Diğer bir deyişle, araştırmacı bu metotla hedeflenen DNA bölgelerini önceden bilmemektedir (o nedenle, tekniğin adı “anonim”’dir). Buna rağmen, bu teknik genetik çeşitliliğin ve farklılaşmanın temel basamakları hakkında oldukça zengin bir bilgi kaynağı sunar.
AFLP belirteçleri, popülasyon veya türlerin farklılıklarının ortaya konmasında ilk basamak olarak kullanılır. AFLP’lerin dezavantajı ise sunabildiği bilgi türünün biraz sınırlı olmasıdır. Örneğin, bu belirteçlerin kökeni ve nükleotid dizilimi bilinmediğinden (belirteçler genom içerisinden farklı uzunluktaki parçalardan oluşmuştur) bir grup organizmanın evrimsel tarihini oluşturmada sınırlıdır.
Buna ek olarak, AFLP belirteçlerinden sıklıkla dominant belirteçler olarak da bahsedilir ve jeldeki bantların, genotipin homozigot (AA) mu yoksa heterozigot (Aa) mu olduğunu belirlemede yetersiz olduğu durumlarda, "var" ya da "yok" olarak skorlanır. Bunun sebebi, AFLP parçalarının her bireyde olan veya olmayan, varsa da tek bir alelin çoğaltıldığı özgün kesim bölgelerini temsil etmeleridir, o nedenle de elde edilebilecek bilgiyi sınırlamaktadır.
Diğer bir benzer metot olan RAPD (Random Amplified Polymorphic DNA- rastgele çoğaltılmış polimorfik DNA) ile de agaroz jel elektroforezinde görülebilir dominant belirteçler elde edilir. Ancak bu metot yerini, görüntüleme tekniklerinin kemilüminesans ve genetik analizleme cihazları ile yapıldığı AFLP tekniğine bırakmıştır.
Diğer belirteç sınıfı, sekans-işaretli bölge belirteçleri (STS- sequence-tagged site) olarak adlandırılır ve türler arası ve tür içi genetik farklılıkların karakterizasyonunda alternatif bir yaklaşım sunar. Sekans-işaretli bölge, genom içerisinde eşi olmayan 200-500 bazçiftlik bir bölgedir ve primerleri araştırmacı tarafından tasarlanan PCR ile belirlenir.
Bir tip STS belirteçleri mikrosatellit bölgelerdedir ve aynı zamanda SSRs (simple sequence repeats- tek sekans tekrarları) veya VNTRs (variable number tandom repeats- değişken sayılı bitişik tekrarlar) olarak da adlandırılırlar. AFLP’lerden farklı olarak bu belirteçler için genellikle DNA’nın kodlanmayan bölgelerinde görülen, “ATC” veya “GAG” gibi ardışık tekrarlanan nükleotid motiflerinin yerlerinin önceden bilinmesi gerekir. Bu bölgelerin, oraya özgü tasarlanacak primerler ve PCR ile çoğaltılmasıyla, STS metodu bize bireyler arasında farklılıkları daha detaylı olarak gösterir.
Ko-dominant belirteçlerde olduğu gibi, belli bir lokus (DNA bölgesi) için bireyin homozigot veya heterozigot (Aa/AA) olduğunu söyleyebilir çünkü PCR sırasında her iki alel (A ve a) de çoğaltılır. Her ne kadar her tekrar, örneğin ATC’lerden oluşsa bile, bütün nükleotid bileşeni tam olarak bilinmediğinden bu belirteçlerin de AFLP’ler gibi filogenetik tanımlama için benzer kısıtlılıkları vardır çünkü belirteç homolojisi bilinmemektedir. Nükleotid bileşenlerinin tam olarak bilinmediği STS belirteçlerini daha işe yarar kılmanın yolu, polimorfik lokuslardan elde edilmiş sekans (dizi) parçalarıdır.
SCARs (sequence characterized amplified regions- dizi tanımlı çoğaltılmış bölgeler) denilen bir belirteç metodu, tam nükleotid kompozisyonunu belirlemek için klonlanmış ve sekanslanmış (dizilenmiş) parçaları kullanır. Bir kez sekanslama yapıldığında, primerler SCAR bölgelerinin etrafına gelecek şekilde tasarlanır ve agaroz jelde uzunluk polimorfizmlerini görebilmek için tekrar çoğaltılır. Enteresan şekilde, bu teknik, işlevselliğini de arttırmak için, sıklıkla AFLP’ler ve RADP’ler gibi anonim ve dominant belirteçlerle birlikte kullanılır.
Moleküler ekologların kullandığı bir diğer seçenek, PCR temelli bir metot olmayan, allozim analizidir. Bu belirteçler, örneğin glikoliz gibi metabolik süreçlerde iş gören enzimlerin kodlandığı bölgelerden elde edilir. STS belirteçlerindeki kadar hızlı evrimleşmemelerine rağmen bu enzimler, organizmaya bağlı olarak, genetik çeşitliliği orta basamaklarından yüksek basamaklarına taşır. Her halükarda, STS veya allozim belirteçleri, eğer popülasyonlar arasındaki heterozigotluk ekolojik çeşitlilikle ilişkiliyse bunu gösterebilir. Örneğin bitkilerde büyüme hızı ve etkinliğiyle ilişkili heterozigotluk dereceleri veya hayvanlarda çevresel koşullara bağlı adaptif cevap (uyum cevabı) incelenebilir.
Moleküler ekologlar tarafından kullanılan üçüncü sınıf belirteçler, genom içerisinde hedeflenen DNA bölgelerinin direk sekanslanmasından türetilmiş olanlardır. Bunlar genellikle Sanger sekanslama olarak adlandırılır (Şekil 5). STS belirteçleri ile olduğu gibi, özel genler veya gen bölgelerinin ilgilenen araştırmacı tarafından önceden bilinmesine ihtiyaç duyulur. İyi tasarlanmış primerler ve PCR ile, bu metot moleküler, ekoloğa bugünün mevcut en temel ve en ince genetik detaylarını sunabilir.
Bunun sebebi, varyasyon derecelerine bağlı olarak, şubeden türe kadar geniş bir aralıkta, bir popülasyondaki bireyler arasında bile, çapraz karşılaştırmaların yapılması için tam nükleotid sekanslarının elde edilebilir olmasıdır. Bu nedenle, bir grup organizmanın evrimsel tarihi ve adaptif özellik bölgelerinin (örneğin bitkilerde gün ışığına duyarlı genlerin olduğu bölgeler) genetik temeli gibi evrimsel süreç ve modelleri anlamada, hayvan türlerinin tarihsel dağılım ve göç tablolarında (örn; Pleistosen’den günümüze kadar), taksonomik sınıflandırmada iş gören özel karakterlerin evrimini anlamada (örn; en temel canlıdan omurgalılara kadar “notokord”un orijini) DNA sekanslama ideal bir yöntemdir.
Hayvan filogenetiği çalışan moleküler ekologların sıklıkla kullandığı işe yarar bir genom da mitokondri DNA’sıdır (mtDNA). mtDNA’nın bir bölgesi, özellikle alt taksonomik basamaklara (tür düzeyi) ait bilgi edinmemizi sağlayan sitokrom oksidaz (cytochrome oxidase- COI) bölgesidir. Aynı zamanda bu bölge, ortak primerlerin kullanılabilmesi ve çeşitli türlerin genetik olarak “barkodlanmasını” sağladığı için “bar-coding” bölgesi olarak da adlandırılır.
Bitki moleküler ekolojistlerin sıklıkla kullandığı bir diğer genom da, bitki göçünün tarihsel izlerinin takibinde ve bitki filogenisinin oluşturulmasında kullanılan, kloroplast genomudur.
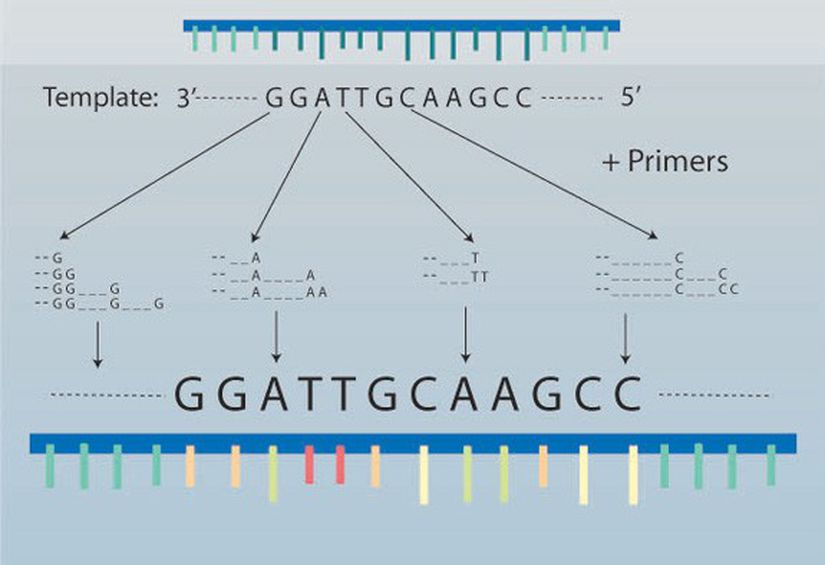
DNA sekanslama, bir diğer oldukça polimorfik kodominant marker tipi olan tek nükleotid polimorfizmlerine (single nucleotide polymorphism-SNPs) de katkıda bulundu. Tek bir türe ait birden fazla bireyde bir bölgenin çoklu sekansları çıkarıldığında, bireyler arasındaki tek baz değişiklikleri saptanır. DNA sekanslamasının derecesine bağlı olarak (belirli bölgeler veya bütün bir genom) SNP’ler, çeşitliliğin basamaklarını gösterebilir ve belirteç homolojileri bilindiğinden filogenetik ağaç oluşturulmasını sağlayabilir. Özel gen bölgelerini hedefleyen bir diğer farklı ama yakın yaklaşım, tüm genom sekanslamasıdır.
Yeni nesil sekanslama (next-generation sequencing) adı verilen yeni geliştirilmiş teknik sayesinde küçük sekanslanmış segmentlerle tüm genom derlenip analiz edilebilmektedir. Bakteri veya virüs gibi küçük genomlu organizmalarla sınırlı olsa da yeni nesil sekanslama, ekoloji temelli sorularına tüm genom üzerinden cevap arayan moleküler ekologlar için önemli bir teknik haline gelmiştir.
Farklı moleküler genetik tekniklerin güçlü ve zayıf tarafları göz önüne alındığında ekolojik bir soruya yanıt aramada hangi deney tasarımının en iyi olacağı merak edilebilir. Bu konu, belirteçler hakkında bilgi ve metot dağarcığının dikkatli değerlendirilmesini gerektirir.
Deney Tasarımı: Rastgele Moleküllerden Uygun Metotlara
Genetik tekniklerle çalışırken sorulacak anahtar soru “Hangisi benim sorum için en iyi bilgiyi sunar?” sorusudur. Bu sorunun cevabı, başarılı bir moleküler ekoloji çalışması ortaya koyabilmek için bütün tekniklerin birlikte ve ayrı ayrı değerlendirilmesinin gerektiği birçok faktör tarafından belirlenmiştir. Şekil 6, hangi metot veya metotların sizin sorunuza en iyi yanıtı verebileceğini gösteren bir akış çizelgesini gösteriyor. Bu soruyu ele almanın birçok farklı yol olsa da, izlenecek bir strateji de araştırmanın taksonomik basamağından başlamaktır.
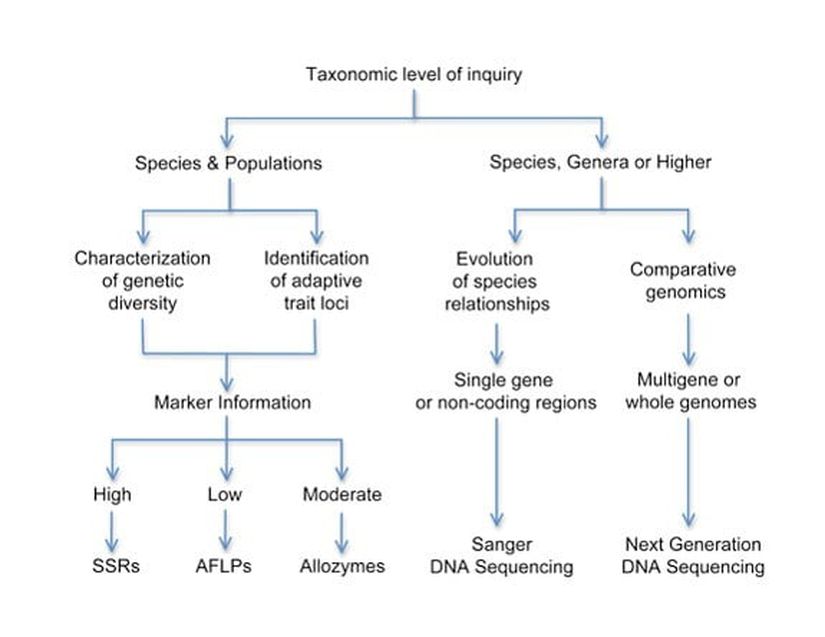
Türler içerisinde popülasyon düzeyindeki farklılıklarla mı ilgileniyorsunuz? İlgilendiğiniz organizma için yalnızca anonim belirteçler mi uygun? O zaman AFLP belirteçleri seçiminiz olabilir.
Gözlenen ya da beklenen heterozigotluklar hakkında detaylı bilgiye mi ihtiyacınız var? Veya bir çevresel değişkenle bir nötral belirteç arasında ilişki bulmaya mı çalışıyorsunuz? O halde AFLP’ler kullanılabilir fakat STS veya allozim belirteçler daha işe yarar olacaktır.
Bir grup organizmanın evrimsel tarihini ortaya çıkarmakla mı ilgileniyorsunuz? Öyleyse; bir cins içindeki türler arasında mı, cinsler arasında mı, yoksa daha yüksek taksonomik basamaklarla mı ilgileneceksiniz (familya, phyla)? Hedefleyeceğiniz bölgeye bağlı olarak [kodlanan veya kodlanmayan DNA, çekirdek veya organel DNAsı] DNA sekanslamadan türetilmiş homolog belirteçler kullanmak seçilecek yöntemlerden en büyük hisseyi alacaktır.
İlgi alanlarınız genom evrimi etrafında mı dönüyor? Örneğin, patojen veya patojen olmayan bakteri genomlarının nasıl farklılaştığını veya patojenlikle ilişkili gen virülansının (öldürücülüğünün) çevresel veya ekolojik ilişkisinin olup olmadığını mı anlamak istiyorsunuz? O zaman şimdilerde küçük genomlar için kolaylıkla yapılabilen tüm genom sekanslama yöntemi size zengin bir bilgi kaynağı sunacaktır.
Hangi belirtecin hangi soru için en iyi yöntem olacağını değerlendirmede birçok farklı yol olsa da, hangi taksonomik basamağa veya hangi genetik varyasyon düzeyine ihtiyacınız olduğu hakkında etraflıca düşünmek en iyi yaklaşımı seçmek için önemli olacaktır. Bu en basit stratejiyi anlamak ve dikkatlice uygulamak, sonunda moleküler ekoloji alanında hangi sorunun yanıtlanabilir ve yayınlanabilir olduğunu belirleyebilir.
İçeriklerimizin bilimsel gerçekleri doğru bir şekilde yansıtması için en üst düzey çabayı gösteriyoruz. Gözünüze doğru gelmeyen bir şey varsa, mümkünse güvenilir kaynaklarınızla birlikte bize ulaşın!
Bu içeriğimizle ilgili bir sorunuz mu var? Buraya tıklayarak sorabilirsiniz.
Soru & Cevap Platformuna Git- 2
- 2
- 1
- 0
- 0
- 0
- 0
- 0
- 0
- 0
- 0
- 0
- Çeviri Kaynağı: Nature Education | Arşiv Bağlantısı
Evrim Ağacı'na her ay sadece 1 kahve ısmarlayarak destek olmak ister misiniz?
Şu iki siteden birini kullanarak şimdi destek olabilirsiniz:
kreosus.com/evrimagaci | patreon.com/evrimagaci
Çıktı Bilgisi: Bu sayfa, Evrim Ağacı yazdırma aracı kullanılarak 20/04/2024 18:17:15 tarihinde oluşturulmuştur. Evrim Ağacı'ndaki içeriklerin tamamı, birden fazla editör tarafından, durmaksızın elden geçirilmekte, güncellenmekte ve geliştirilmektedir. Dolayısıyla bu çıktının alındığı tarihten sonra yapılan güncellemeleri görmek ve bu içeriğin en güncel halini okumak için lütfen şu adrese gidiniz: https://evrimagaci.org/s/429
İçerik Kullanım İzinleri: Evrim Ağacı'ndaki yazılı içerikler orijinallerine hiçbir şekilde dokunulmadığı müddetçe izin alınmaksızın paylaşılabilir, kopyalanabilir, yapıştırılabilir, çoğaltılabilir, basılabilir, dağıtılabilir, yayılabilir, alıntılanabilir. Ancak bu içeriklerin hiçbiri izin alınmaksızın değiştirilemez ve değiştirilmiş halleri Evrim Ağacı'na aitmiş gibi sunulamaz. Benzer şekilde, içeriklerin hiçbiri, söz konusu içeriğin açıkça belirtilmiş yazarlarından ve Evrim Ağacı'ndan başkasına aitmiş gibi sunulamaz. Bu sayfa izin alınmaksızın düzenlenemez, Evrim Ağacı logosu, yazar/editör bilgileri ve içeriğin diğer kısımları izin alınmaksızın değiştirilemez veya kaldırılamaz.
This work is an exact translation of the article originally published in Nature Education. Evrim Ağacı is a popular science organization which seeks to increase scientific awareness and knowledge in Turkey, and this translation is a part of those efforts. If you are the author/owner of this article and if you choose it to be taken down, please contact us and we will immediately remove your content. Thank you for your cooperation and understanding.




